Propiedades coligativas
- BENJAMIN GUAJARDO
- 1 jun 2020
- 2 Min. de lectura
Las propiedades coligativas son las propiedades de las disoluciones, las cuales dependen de la cantidad de soluto no volátil en relación al solvente.
¿Que es la volatilidad?
Las moléculas de los líquidos siempre están en movimiento y a veces suelen escaparse en forma de gas. Esto se debe a la poca atracción entre las moléculas.
Menor atracción - Mayor volatilidad
Mayor atracción - Menor volatilidad
Como bien sabemos, las disoluciones no presentan una reacción química, entonces ¿Porque la presencia de un soluto cambia las propiedades de un solvente?
Esto ocurre porque el soluto atrae al solvente, generando una mayor fuerza de atracción y dando paso a las siguientes propiedades:
Disminución de la presión de vapor
Esta se puede calcular con la Ley de Raoult:
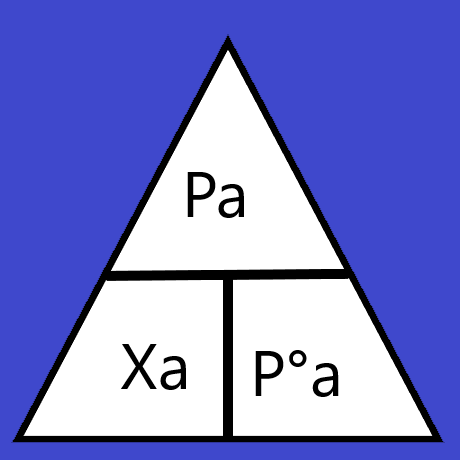
En donde:
Pa = Presión de vapor del solvente.
Xa = Fracción molar del disolvente.
P°a = Presión de vapor del solvente puro.
Esta fórmula solo aplica para disoluciones con solutos no volátiles.
¿Que hay de las soluciones con solutos y solventes volátiles?
La formula es la siguiente:

Pt = Presión de vapor total.
P = Presión de vapor en disolución.
P° = Presión de vapor componente puro.
X = Fracción molar.
Aumento del punto de ebullición
Todos entendemos por punto de ebullición como la temperatura a la que hierve un líquido, y es correcto, pero otra forma de interpretarlo es la temperatura a la que la presión de vapor iguala la presión atmosférica. Esto explica por qué el agua hierve a distintas temperaturas dependiendo de la altura en la que nos encontremos.
El aumento del punto de ebullición se puede obtener con la siguiente fórmula:

ΔT = Aumento del punto de ebullición.
kb = Constante ebulloscópica.
m = Molalidad.
Tb = Punto de ebullición de la solución.
T°b = Punto de ebullición del solvente puro.
Disminución del punto de fusión
El punto de fusión (o de congelación) de una solución SIEMPRE será menor que el punto de fusión de su solvente puro.
La formula es muy similar a la anterior:

ΔTc = Disminución del punto de congelación.
kc = Constante crioscópica.
m = Molalidad.
T°c = Punto de C. del solvente puro.
Tc = Punto de C. de la solución.
Presión osmótica
Ya hablé de la ósmosis en ¿Por que el agua salada nos da sed?. Podemos definir la presión osmótica como la presión necesaria para detener la ósmosis.
Su formula es:

π = Presión osmótica.
M = Molaridad.
R = constante de los gases ideales (0,082 atm/mol).
T = Temperatura (Kelvin).

Comentarios